En los primeros cursos de grados biosanitarios es normal llegar a las primeras clases de laboratorio sin saber en qué consisten algunas de las técnicas que se van a utilizar para realizar las prácticas. En este artículo vamos a profundizar en dos técnicas de uso común en el laboratorio para tratar de ofrecer una base de la que partir. Las técnicas escogidas son: Centrifugación y Electroforesis.
Centrifugación
Una de las técnicas que primero utilizamos en el laboratorio es la centrifugación. La centrifugación utiliza una fuerza giratoria para separar elementos de diferentes densidades y esta fuerza giratoria se consigue con una máquina llamada centrifugadora o centrífuga.
En las prácticas de grados biosanitarios la centrifugación es útil para separar y analizar componentes de una muestra fluida. Los componentes, dependiendo de la muestra, pueden ser: diferentes tipos de células, fragmentos celulares, orgánulos, etcétera. Esto es posible debido a que los componentes de una muestra fluida tienen diferencias en cuanto a tamaño, peso y densidad.
Generalmente, utilizaremos una microcentrífuga en la que introduciremos tubos comúnmente llamados Eppendorf. Una vez realizada la centrifugación en el tubo distinguiremos dos fases: una sólida al fondo del tubo (la que ha sedimentado) y una líquida. A partir de aquí, dependiendo de nuestro protocolo, avanzaremos en una dirección o en otra.
Existen muchos tipos de centrifugadoras, de diferentes tamaños y con diferentes funcionalidades, por lo que en función de las condiciones de la centrifugación (también teniendo en cuenta las características del medio y de las partículas en él) tendremos un tipo u otro dentro de la misma técnica. Algunos ejemplos: diferencial, isopícnica y zonal.
 Imagen de una microcentrífuga con capacidad para seis tubos. (Sarahi.gutierrezf / CC BY-SA
Imagen de una microcentrífuga con capacidad para seis tubos. (Sarahi.gutierrezf / CC BY-SA
(https://creativecommons.org/licenses/by-sa/3.0))
Electroforesis
La electroforesis es una técnica que nos permite la separación de moléculas aplicando un campo eléctrico. La separación es posible ya que la mayoría de macromoléculas están cargadas eléctricamente y, generalmente, en las prácticas que se realizan en grados biosanitarios, la separación se produce a través de lo que se denomina una matriz porosa (electroforesis en gel). Existen otros tipos de electroforesis: sobre una superficie hidrata en un soporte sólido (por ejemplo, electroforesis en papel) o en una disolución (electroforesis libre).
La electroforesis a través de una matriz porosa, requerirá que preparemos nosotros el gel, generalmente de agarosa. Cuando el gel esté preparado y colocado en la cubeta de electroforesis, introduciremos la muestra que pretendemos separar en los diferentes pocillos (huecos que estarán formados en el gel gracias a la peineta que habremos puesto mientras lo preparábamos) y al acabar aplicaremos el campo eléctrico para que se inicie el proceso.
La separación de moléculas que observaremos en el gel se deberá, además de a la diferencia de potencial eléctrico, a la masa de las moléculas analizadas: las moléculas más ligeras avanzarán más deprisa en el gel y las más pesadas tenderán a situarse en la parte superior del gel. Gracias a ello (y gracias a un marcador de referencia) podremos determinar aproximadamente los pesos moleculares de nuestras moléculas o fragmentos moleculares. Esto nos permitirá realizar multitud de experimentos con proteínas y ácidos nucleicos.
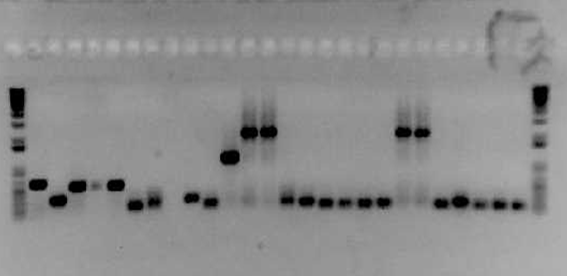 Ejemplo de gel de electroforesis. Cada línea en las diferentes columnas muestra, en este caso concreto, un fragmento de ADN. La primera y la última columna contienen el marcador, que sirve de guía para poder determinar los pesos moleculares de las muestras analizadas.
Ejemplo de gel de electroforesis. Cada línea en las diferentes columnas muestra, en este caso concreto, un fragmento de ADN. La primera y la última columna contienen el marcador, que sirve de guía para poder determinar los pesos moleculares de las muestras analizadas.



